|
|
Determinación Inmunohistoquímica del HER2 en una muestra de pacientes con cáncer de mama del INOR.
Lic. Rosa Irene Alvarez Goyanes
,
Lic. Xiomara Escobar Perez
,
Dr. Rolando Camacho Rodríguez
,
Téc. Maiby Orozco López
,
MsC Leticia Llanes Fernández
,
PhD Julia Cruz Mojarrieta
,
Téc. Maria Emilia Juliá Rodríguez
y
Lic. Martha Guerra Yi
Laboratorio Inmunohistoquimica Experimental
Instituto Nacional de Oncologia y Radiobiologia
29 y F Vedado
10400
Ciudad de la Habana
Cuba
|
|
|
|
|
|
|
|
Resumen
|
|
|
|
Introducción: El receptor del factor de crecimiento humano 2 (HER2), también conocido como c-erbB-2 o HER2/neu, es una proteína perteneciente a la familia del receptor del factor de crecimiento epidérmico. Su amplificación / sobreexpresión y la alteración del gen se han encontrado en más del 20% de los tumores de mama humano, asociándose con el crecimiento tumoral agresivo y con mal pronóstico. Actualmente se considera esta molécula un factor de posible valor pronóstico y predictivo en cáncer de mama.
Objetivo: Conocer la frecuencia de la sobreexpresión de esta proteína en las muestras tumorales de las pacientes con cáncer de mama.
Materiales y Métodos: En el laboratorio de Inmunohistoquímica experimental del Instituto de Oncología y Radiobiología, se determinó la expresión de esta proteína en una muestra de 101 casos de pacientes con cáncer mamario, los cuales se seleccionaron durante un período de 4 meses. Se utilizó la técnica de IHQ mediante el empleo del juego diagnóstico HercepTest TM ( Dako ).
Conclusiones: En nuestro estudio encontramos un 28% de sobreexpresión de la proteína, lo que se corresponde con el reportado en la literatura para esta localización tumoral, el cual oscila entre 20 – 30 %.
|
|
|
|
|
|
|
Introducción
|
|
|
|
El receptor del factor de crecimiento humano 2 (HER2), también conocido como c-erbB-2 o HER2/neu, es una proteína perteneciente a la familia de los receptores del factor de crecimiento epidérmico. Actualmente ocupa un importante lugar como marcador tumoral con posible valor pronóstico y sobre todo predictivo para el cáncer de mama. El gen HER2 puede estar amplificado y su receptor proteico sobre expresado entre un 20-30% de los tumores de mama, lo que indica que puede jugar un importante papel en la malignización celular(1).
Está generalmente aceptado que la sobreexpresión de HER2 se asocia con un crecimiento tumoral agresivo y con mal pronóstico en el cáncer invasivo de la mama, particularmente en la enfermedad con ganglios metastásicos (2). Clínicamente la sobreexpresión y/o amplificación del HER2 en el cáncer de mama esta asociado con los tumores RE negativos, anomalías de la p53, bcl-2 negativos, alto índice mitótico e infiltración linfoide y respuesta reducida a la quimioterapia y la terapia hormonal (1),sin embargo, no ha sido posible llegar a conclusiones definitorias sobre el impacto del HER2 en la respuesta a la terapia endocrina o quimioterapia.
La positividad de HER2 predice una disminución de la respuesta a la terapia hormonal especialmente al tamoxifen. La relación entre el estatus del HER2 y la quimioterapia es mas débil y menos definida. Algunos estudios sugieren que predice sensibilidad al tratamiento con las antraciclinas y la resistencia a la terapia con CMF, aunque, existen estudios que muestran resultados contradictorios. Su valor como marcador tumoral predictivo de respuesta esta en el uso de tratamientos “diana”como el Trastuzumab (3).
En la práctica la IHQ es el método mas usado para determinar el estatus del HER2, permitiendo la identificación de la sobreexpresión de la proteína en las células tumorales individualmente (2).
|
|
|
|
|
|
|
Material y Métodos
|
|
|
|
El estudio incluyó 101 pacientes con carcinoma ductal infiltrante de la mama cáncer de mama, atendidos en el Instituto Nacional de Oncología y Radiobiología . Se utilizaron fragmentos de tejidos fijados en formalina y embebidos en parafina del Departamento de Anatomía Patológica.
Mediante el método Inmunohistoquímico se determinó la sobreexpresión de la proteína HER2, con este fin se empleo el juego diagnóstico para determinación de HER2, DAKO Hercep Test TM.
De cada caso se tomo una lámina con 2 cortes de 4 micras de espesor cada uno, los que se montaron sobre láminas silanizadas, las cuales se incubaron a 68oC durante 12 horas.
Los cortes de tejidos fueron desparafinados en xilol e hidratados en etanol a concentraciones decrecientes, aclarados durante 5 minutos (min ) en H2O bidestilada y lavados en solución salina tamponada con fosfatos (SSTF). Se realizó el desenmascaramiento antigénico del HER2 hirviendo las láminas en buffer citrato pH 6,8 durante 40 min, utilizando un horno microondas. Los cortes se dejan enfriar durante 20 min, se lavan con agua destilada y posteriormente en solución SSTF. La peroxidasa endógena se inhibió con una solución de H2O2 al 3% durante 5 min a temperatura ambiente ( TA ), se lavo con SSTF , aplicándose el anticuerpo anti- HER2 y el control negativo (SSTF) durante 30 min a TA , después del lavado se utilizó el reactivo de visualización durante 30 min, después del lavado finalmente se aplica a las secciones de tejido una mezcla fresca de una solución de 3,3’-diaminobencidina ( DAB ) en 1ml de buffer sustrato durante 10 min, contrastándose con Hematoxilina de Mayer, seguida de deshidratación en los alcoholes a concentraciones ascendentes , clarificación en xilol y finalmente se monta en medio permanente Eukitt ( Kinder GmbH & CO ). En cada experimento se usó una lámina control positivo del DAKO Hercep Test TM que contiene tres clones celulares, con diferente expresión de la oncoproteína HER2 y en ocasiones se utilizaron controles alternativos.
La evaluación se realizó de forma semicuantitativa utilizando un microscopio de luz blanca ( Leica ) y el marcaje se clasificó según la Guía para el uso del Herceptest, propuesta por la DAKO y aceptada por la FDA:
Negativo( 0 ) , ausencia de coloración en toda o parte de la membrana citoplasmática, coloración en <10% de las células tumorales.
Negativo( +1 ) , fina barrera de coloración en parte de la membrana citoplasmática, coloración > 10% de las células tumorales.
Ligeramente positivo ( +2 ), leve a moderada coloración en toda la membrana citoplasmática en > 10% de las células tumorales.
Fuertemente positivo ( +3 ), moderada a fuerte coloración en toda la membrana citoplasmática en > 10% de las células tumorales.
|
|
|
|
|
|
|
Resultados
|
|
|
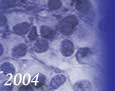
Como podemos apreciar en la tabla I , en las 101 muestras estudiadas encontramos representado todo el patrón de marcaje reportado para esta proteína, como se muestra en las figuras 1 ( a,b,c y d ). De los 101 casos estudiados, 67 resultaron negativos con marcaje 0, en los que se observo ausencia total de marcaje en toda o parte de la membrana en < del 10% de las células, otro grupo de 6 pacientes se clasificaron también negativos pero con un marcaje 1+, encontrándose una coloración en fina barrera en parte o en toda la membrana en mas del 10% de las células. De los grupos positivos, 7 muestras fueron clasificadas como ligeramente positivas con una escala de 2+ por presentar leve o moderada tinción en toda la membrana citoplasmática, así como 21 de las muestras estudiadas se encontraron fuertemente positivas, 3+ , presentando una coloración de moderada a fuerte en toda la membrana citoplasmática. En ambos grupos se analizaron mas del 10% de las células. Al calcular los por cientos de expresión del marcador en cada uno de los 4 grupos, encontramos que el mayor correspondió a los casos negativos que alcanzaron un 72%. Dentro del grupo de los clasificados como positivos se encontró un 6,93% de los ligeramente positivos y un 20,8 de los 3+ o fuertemente positivos, el porcentaje total de este grupo fue de un 28%, valor que esta comprendido en le rango reportado en la literatura para el mismo, el cual oscila entre 20 - 30% de expresión de esta proteína oncogénica (4,5,6) Es interesante destacar el hecho de que solo en pacientes con marcaje 3+ se esperan altos índices de respuesta al tratamiento con Trastuzumab (7). Tabla 1 | HER2 | Numero de casos | Por ciento ( % ) | | 0 | 67 | 66,34 | | 1+ | 6 | 5,94 | | 2+ | 7 | 6,93 | | 3+ | 21 | 20,8 | | Total | 101 | 100,00 |
|
|
|
|
|
|
|
Discusión
|
|
|
|
En nuestro estudio encontramos un 28% de sobreexpresión del receptor proteico, lo que se corresponde con lo reportado en la literatura para el HER2 en cáncer de mama.
|
|
|
|
|
|
|
Bibliografia
|
|
|
|
1. Dawen X, Xiao- Ou S, Zonglin D, Wan-Quing W, Kim E. C, Qi D, Yu- tang G, Fan J, Wei Z. Population – based, case- control study of Her/2 genetic polymorphism and breast cancer risk. Journal of the National Can. Inst.92; 5: 412- 417, 2000.
2. van de Vijver M. J. Assessment of the need and appropriate method for testing for the human epidermal growth factor receptor- 2 (Her/2). European Journal of cancer. 37: S11-S17, 2001.
3. Piccart M, Lohrisch C, Di Leo A, Larsimont D. The predictive value of Her/2 in breast cancer. Oncology 61; (supp 2): 73-82, 2001.
4. Esteva- Lorenzo F.J, Sastry L, King C.R. The erb B- 2 gene: From research to application, in Dickson R., Salomon D.S ( eds ): Hormones and Growth factors in Development and Neoplasia. New York, N.Y, 1998, pp 421- 444.
5. Slamon D.J, Clark G.M,Wong S,G, Levin W,J,Ullrich A, Mcguire W.L. Human breast cancer: correlation of relapse and survival with amplification of the Her2-2/neu oncogene. Science 1987: 235:177- 182.
6. Salmón D.J, GodolphinW, Jones L.A, , et al. Studies of the Her-2/neu proto oncogene in human breast and ovarian cancer. Science 1989: 244: 707- 712.
7. Slamon D.J, Leyland- Jones B, Shak S, Fuchs H, Paton V, Bajamonde A, Fleming T, Eiermann W, Wolter J, Pegram M, Balsega J, Norton L. Use of chemotherapy plus a monoclonal antibody against her2 for metastatic breast cancer that overexpresses Her2. The New England Journal of Medicine 2001: 344:783- 792.
|
|
|
|
|
|
|
Comentarios
|
|
|
El 23/3/2004 12:18, LIC; ISABEL BROWN dijo:
LA DETERMINACION INMUNOHISTOQUIMICA DEL H. ES MUY IMPORTANTE PARA LOS PACIENTES CON CANCER DE MAMA, ASI QUE ESTE TRABAJO ESTA MUY VALIOSO, DONDE SE VE LOS ADELANTO CIENTIFICO EN EL MUNDO ENTERO Y MUCHO MEJOR AQUI EN NUESTRO PAIS QUE AUNQUE ESTAMOS BLOQUEADO SIEMPRE PENSANDO EN NUESTROS PACIENTES PARA AYUDARLOS A TENER UNA LARGA VIDA. ME GUSTO MUCHO ESE TRABAJO Y ESTA MUY BIEN REALIZADO, YA QUE HE LEIDOS OTROS DE OTROS PAISES
Hacer un comentario a este Trabajo
|
|
|
|